Electrophorèse sur gel d'agarose
Électrophorèse sur gel d’agarose
Migration électrophorétique
Dans le cas des acides nucléiques, ADN et ARN sont uniformément chargés négativement (groupements phosphates ionisés). Donc, les échantillons d'ADN déposés côté cathode, migrent vers l'anode.
Séparation dans le gel d’agarose
Le gel d'agarose est un réseau poreux, ainsi, les échantillons d'ADN migrent plus ou moins vite vers l'anode en fonction de leur encombrement qui dépend :
- de la taille (nombre de paires de bases)
- de la conformation de l'ADN (linéaire, circulaire relachée, superenroulée).
Influence de la taille et de la conformation de l'ADN sur la migration
Taille des fragments
Pour un ADN linéaire, la mobilité électrophorétique est inversement proportionnelle au logarithme du nombre de paires de bases.
Les petits fragments migrent plus vite que les grands fragments.
Conformation de l'ADN
A taille égale :
- l'ADN superenroulé (FI) est le plus compact: migration la plus rapide.
- l'ADN circulaire relâché (FII, FIr) est plus encombrant: migration la plus lente.
- l'ADN linéaire (FIII) présente une migration intermédiaire.
Cas particulier des plasmides
Dans la cellule hôte, les plasmides sont circulaires, double brin et superenroulés.
Lors des manipulation de clonage, les formes FI, FII et FIII peuvent coexister. Il est possible de les séparer par électrophorèse sur gel d’agarose, ce qui permet également:
- de vérifier l'intégrité d'un plasmide,
- de contrôler une digestion enzymatique,
- de détecter des dégradations de l'ADN.
Les figures suivantes illustrent la migration et les conformations plasmidiques.
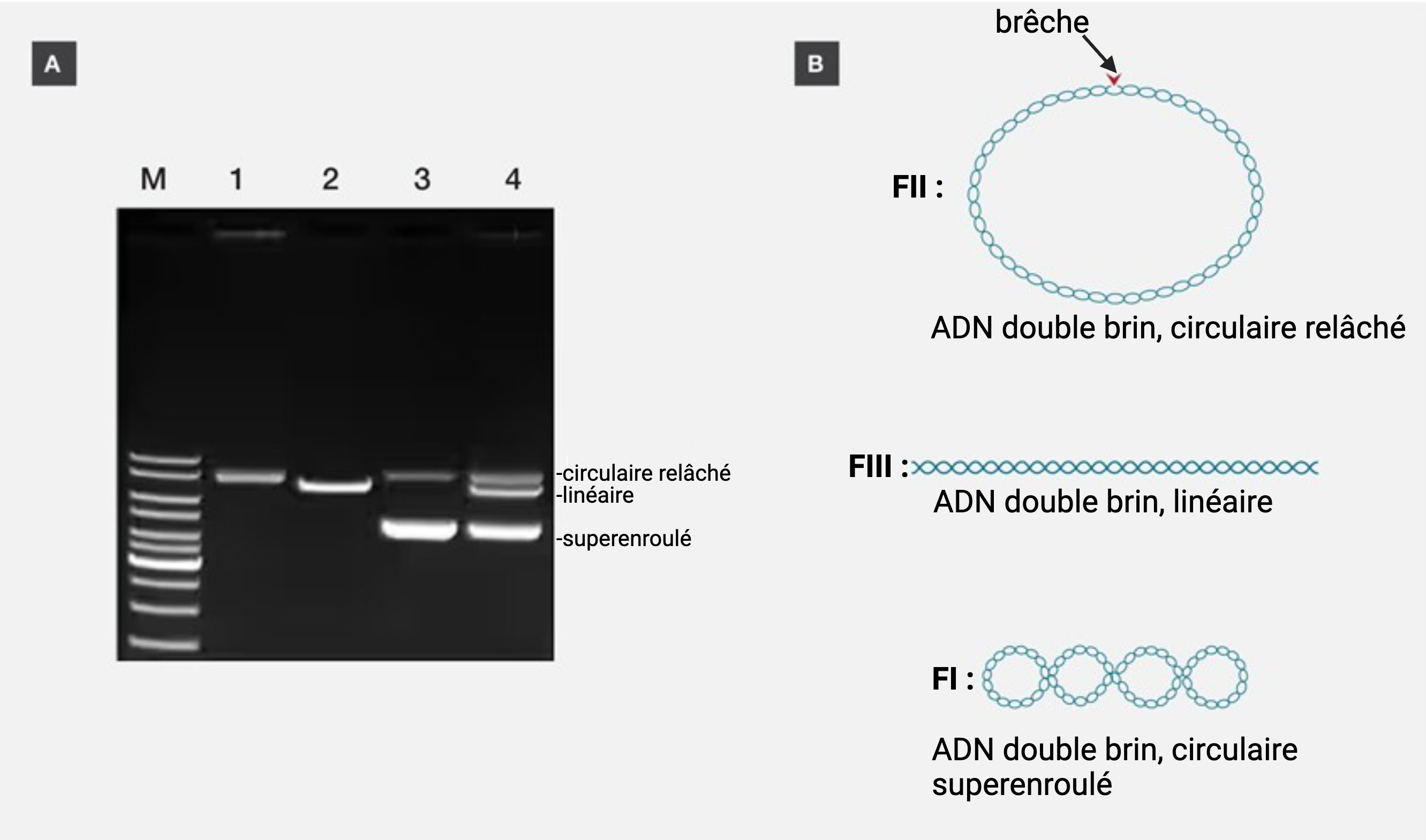
A : Migration élecrophorétique sur gel d'agarose d'un plasmide sous différentes conformation :
- piste M : marqueur de taille,
- piste 1 : forme FII ou FIR circulaire relâchée,
- piste 2 : forme FIII linéaire,
- piste 3 : forme FI superenroulée en bas de la piste, la bande en haut de la piste est de l’ADN qui a été « cassé » et se trouve sous forme FII,
- piste 4 : les 3 formes, de haut en bas FII/FIR circulaire relâchée, FIII linéaire et FI superenroulée.
B : Schémas des différentes conformations d'ADN plasmidique:
De haut en bas :
- (FII) circulaire relachée,
- (FIII) linéaire
- (FI) superenroulée.
Paramètres expérimentaux
Le tampon assure :
- la conduction du courant électrique,
- un pH stable,
- la protection de l'ADN (EDTA chélateur de cations bivalents).
Deux tampons de migration sont couramment utilisés:
- TAE (Tris-Acétate EDTA) :40mM Tris-Acétate/ 1mM EDTA, pH 8.3.
Bonne séparation des grands fragments (>2kpb),
Idéal pour l'extraction d'ADN à partir du gel. - TBE (Tris-Borate-EDTA) : 0.13M Tris pH/45mM acide Borique/ 2.5mM EDTA, pH8.3.
Meilleure résolution des petits fragments (<2kpb),
Tampon stable dans le temps.
Pourcentage en agarose
La concentration en agarose est exprimée en pourcentage (g/100mL).
Ce pourcentage détermine la taille du maillage du gel.
- % éleve = maillage serré = meilleure séparation des petits fragments
- % faible = maillage lâche = adapté aux grands fragments
Résolution des gels d'agarose:
| Pourcentage en agarose | Taille des fragments d'ADN (en pb) |
| 0,5% | 1 000 à 30 000 |
| 0,7% | 800 à 12 000 |
| 1% | 500 à 10 000 |
| 1,2% | 400 à 7 000 |
| 1,5% | 200 à 3 000 |
| 2% | 50 à 2 000 |
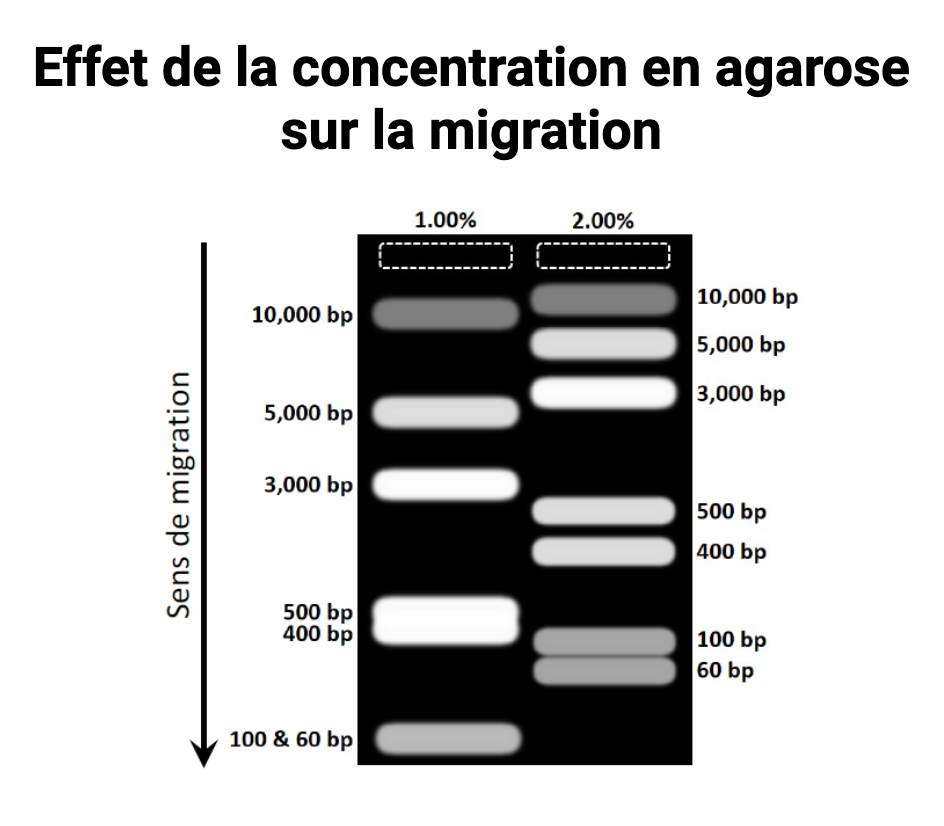
Effet de la concentration d'agarose sur la migration:
- Gel à 1% (à gauche). Mauvaise résolution pour petits fragment (400pb et 500pb ne sont pas séparés).
- Gel à 2% (à droite). Bonne résolution des fragments de petite taille (400bp/500bp d'une part et 100bp/60bp d'autre part sont distincts).
Exemple de protocole expérimental
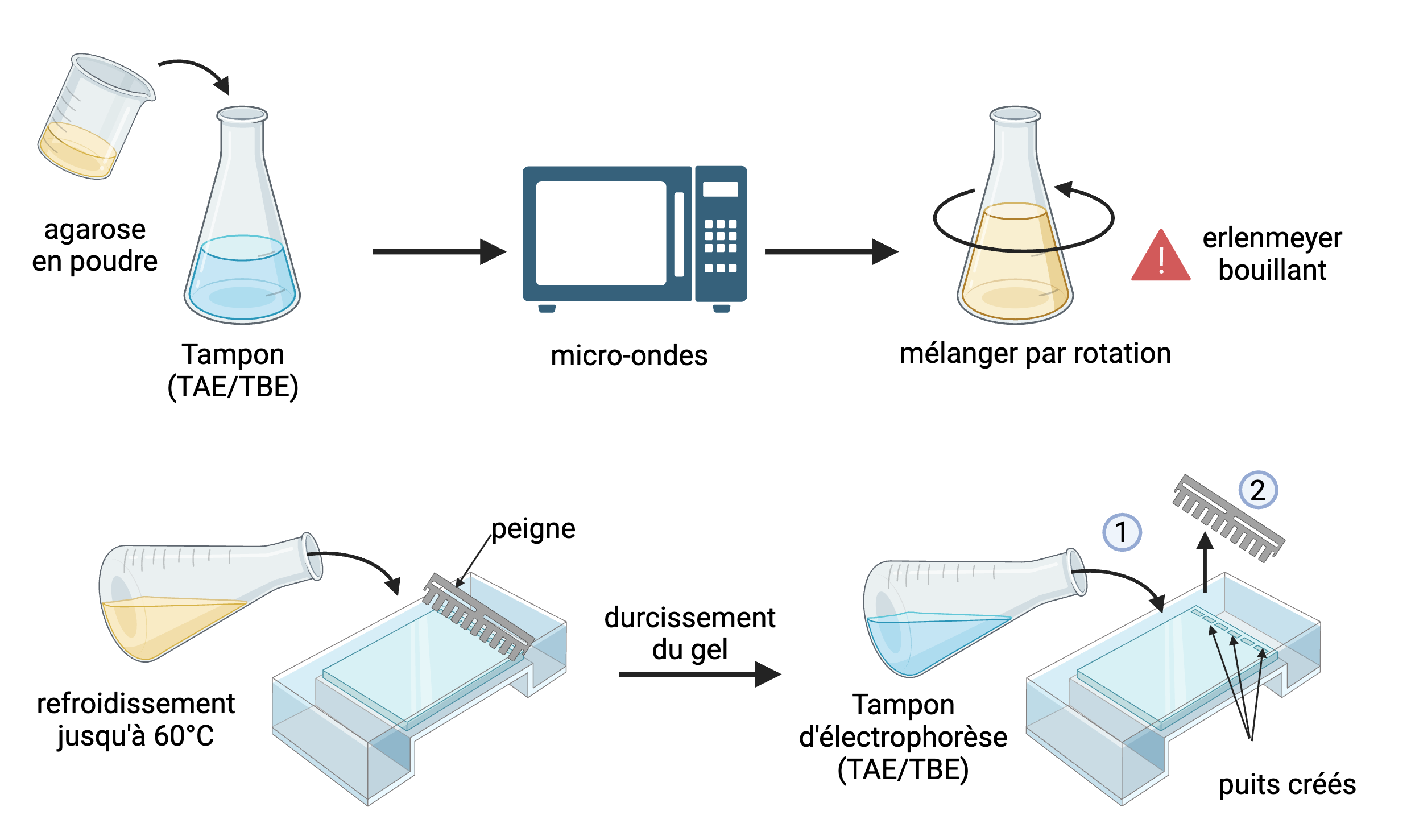
Préparation du gel d’agarose
L'agarose (poudre) est dissoute à chaud dans du TAE ou TBE, puis coulée dans un moule/support muni d'un peigne. Après solidification, le peigne est retiré formant les puits de dépôts.
Préparation des échantillons d'ADN
Les échantillons d’ADN sont mélangés à un tampon de dépôt qui permet:
- d'augmenter la densité (glycérol),
- de visualiser le dépot et la migration (bleu de bromophénol, xylène cyanol),
- de stopper les réactions enzymatiques (EDTA).
Composition et dilution du tampon de dépôt 6X
Composition du tampon de dépôt 6X
- 60% de glycérol
- 0,03% de bleu de bromophénol
- 0,03% de xylène cyanol
- 60 mM EDTA, pH 7,6
Le tampon 6X doit être dilué au 1/6e dans l'échantillon. Autrement dit, il faut mélanger:
- 5 volumes d'échantillon
- pour 1 volume de tampon 6X.
(par exemple, pour un échantillon de 10µL, il faut ajouter 2 µL de tampon 6X).
Dépôt et migration
Les échantillons d'ADN et un marqueur de taille sont déposés dans les puits.
La migration se fait sous tension entre 1 et 5V/cm.
L'électrophorèse est arrêtée avant que ce front de migration (bleu de bromophénol) ne sorte du gel.
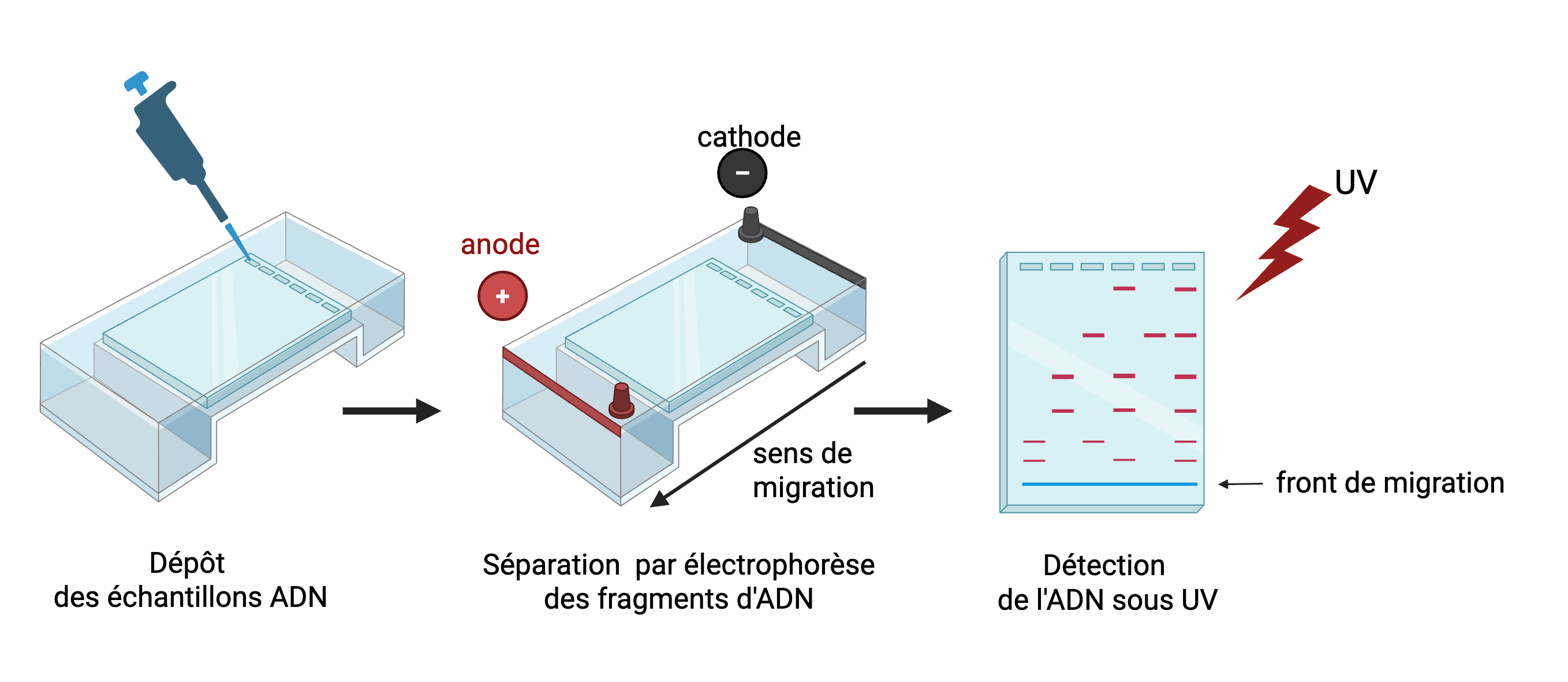
Visualisation des acides nucléiques
L'ADN (incolore) est visualisé grâce à des molécules fluorescentes qui se lient spécifiquement à l'ADN.
Les molécules fluorescentes se concentrent au niveau de l'ADN et émettent une fluorescence détectable sous UV.
L’intensité de fluorescence reflète la quantité d'ADN. Il est possible de de quantifier l’ADN en comparant l’intensité des bandes avec celles du marqueur de taille.

Colorants fluorescents
| Molécule | Mode d'interaction | Fluorescence | Remarques |
| Bromure d'Ethidium | Intercalant | Rouge-orangée | Très sensible, mutagène |
| SYBR GreenTM/ SYBR Safe |
Liaison au petit sillon | Verte | Moins toxique |
Le BEt (mutagène) est aujourd'hui remplacé par des colorants moins toxique mais moins sensible.
Analyse des résultats
Les fragments d'ADN apparaissent dans le gel sous forme de bandes fluorescentes.
On analyse :
- le nombre de bandes par piste
- la position dans le gel (taille)
- leur intensité (quantité)
- la présence de traînée (smear) qui indiquent une dégradation.
Estimation de la taille des fragments
Rôle du marqueur de taille
Un marqueur de taille (ladder), est un mélange de fragments d'ADN de taille connue.
Il permet d'estimer la taille des fragments par comparaison des distances de migration.
Cette estimation n'est valable que pour des fragments linéaires.

Exemples de deux marqueurs de taille:
- Piste A: gene Ruler 1kb de Thermo ScientificTM
- Piste B : Echelle de taille et de masse moléculaire d’ADN de Jeulin
La gamme étalon
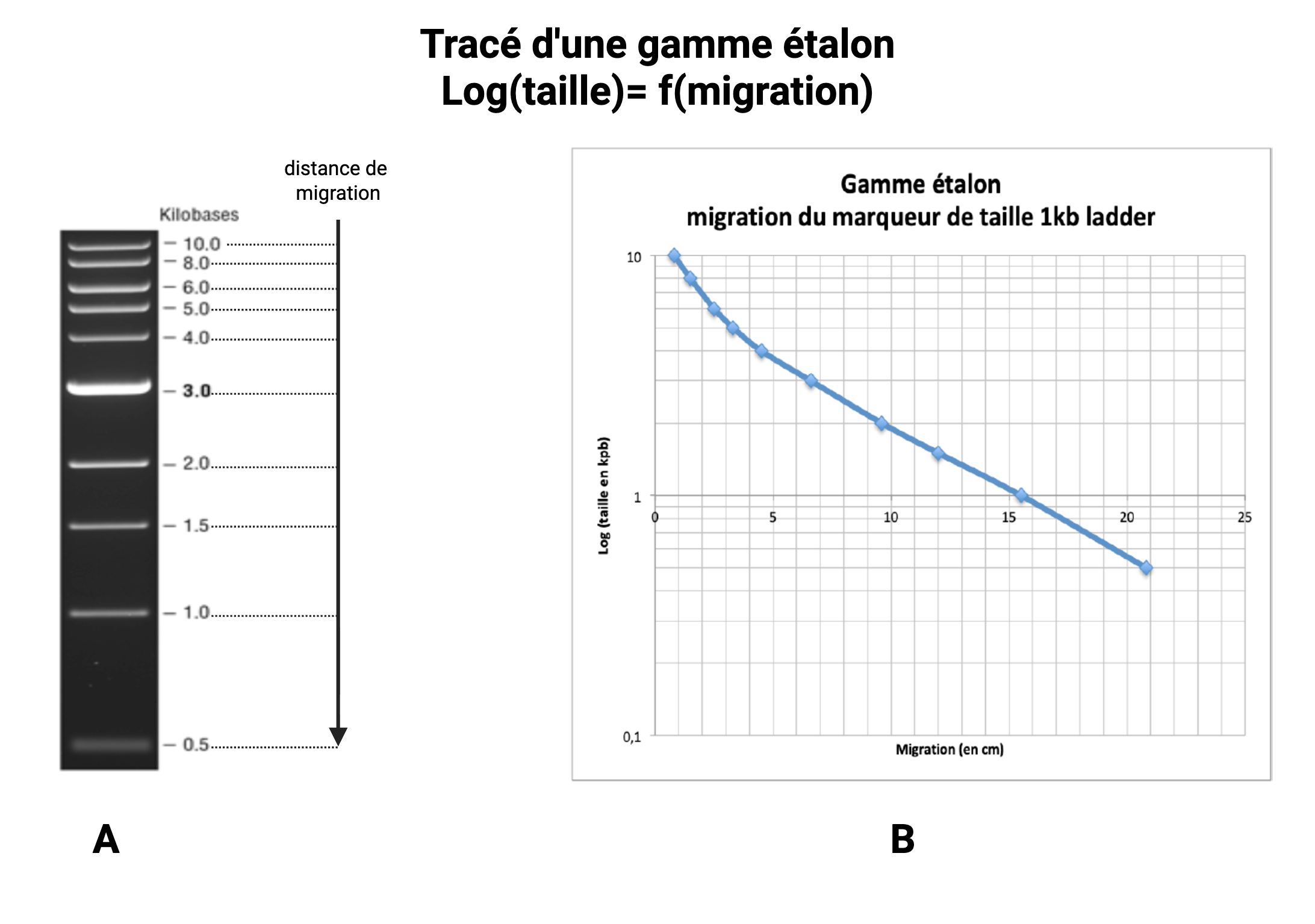
Même si la plupart des extimations des tailles se font à l'oeil nu (voir figure A suivante), il est possible de tracer une gamme étalon pour avoir plus de précision (voir figure B suivante).
Cette courbe relie la distance de migration au logarithme du nombre de paires de bases qui est une relation linéaire SAUF, aux extrémités (pour les plus grands et plus petits fragments), zones où la relation devient moins fiable en raison de résolution du gel qui n'est plus adapté à la taille des fragments (trop concentré pour séparer les plus grands fragments, pas assez concentré pour distinguer les fragments les plus petits)
Quantification
Quantification
L’analyse à l'oeil nu ou par densitométrie (logiciels d’analyse d’image) permet une estimation des quantités avec la comparaisons de l'intensité des bandes de l'échantillon et celles du marqueur de taille dont les quantités sont connues (à condition de faire la comparaison avec une bande de taille voisine).
Cette méthode est moins précise que la spectrophotométrie.







