Vérification des clones par séquençage
Le séquençage de l'ADN consiste à déterminer l'ordre exact des nucléotides (A,T,G et C) d'une molécule d'ADN.
Dans le cadre d'un clonage, le séquençage est généralement réalisé à partir :
- d'un plasmide recombinant purifié,
- en utilisant des amorces localisées dans le vecteur, encadrant le site multiple de clonage (MCS), ce qui permet de lire l'insert.
Rôle du séquençage
Le séquençage constitue l'étape de validation du clonage.
Il permet de vérifier sans ambigüité:
- la fidélité de la séquence clonée,
- l'absence de mutations (substitutions, insertions ou délétions),
- l’orientation correcte de l’insert,
- l’intégrité du cadre de lecture dans le cas d'un clonage d'expression.
Evolution des technologies de Séquençage
Les technologies de séquençage se répartissent en trois grandes générations :
- Première génération : séquençage par terminaison de chaîne (Sanger).
- Deuxième génération (NGS) : séquençage à haut débit.
- Troisième génération (TGS) : séquençage de molécules uniques.
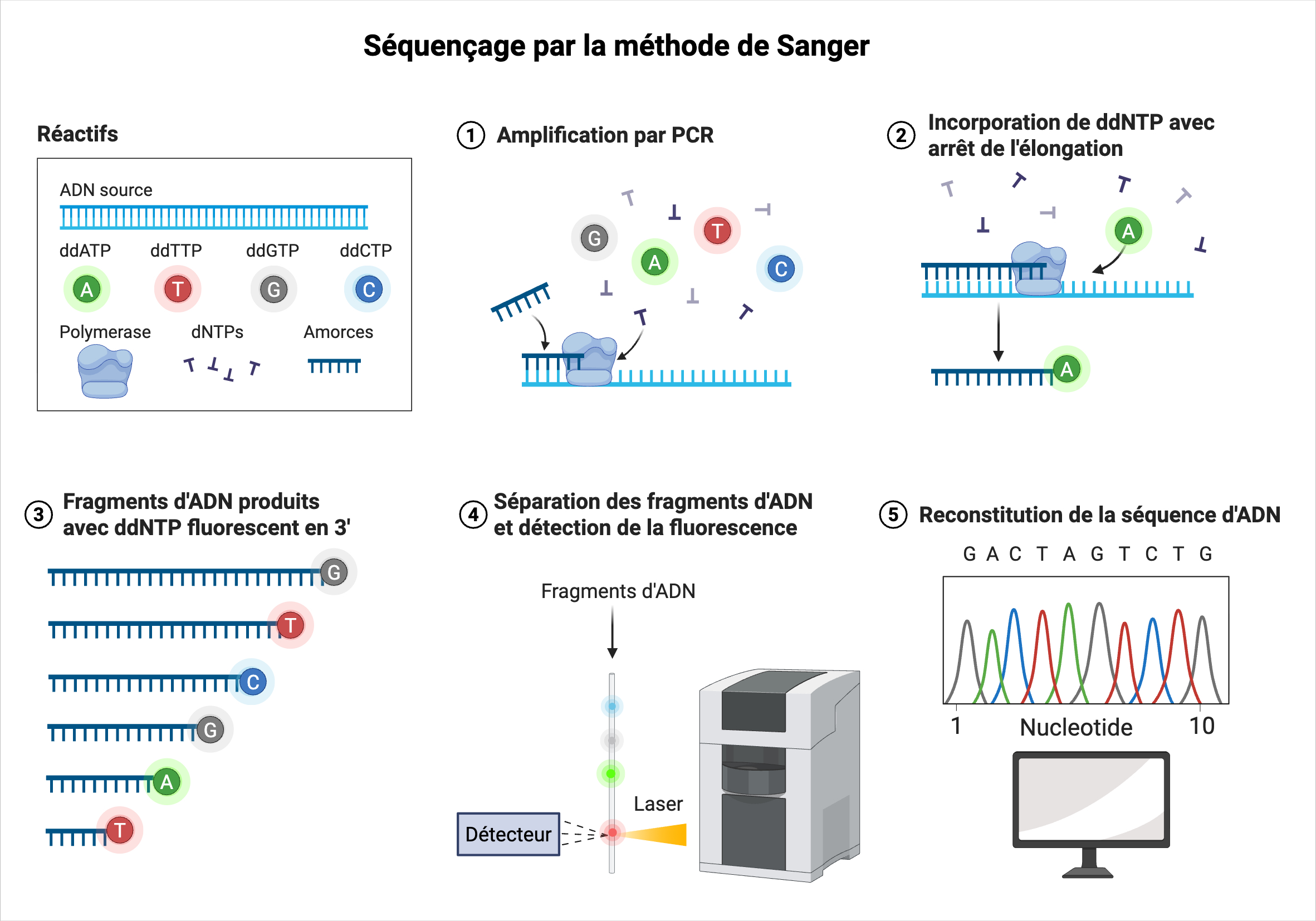
Séquençage de première génération : méthode de Sanger
Développée en 1977 par Frederik Sanger, cette méthode repose sur la terminaison de chaîne lors de la synthèse d'ADN.
La réaction se fait en présence:
- des précurseurs dNTP classiques
- de didésoxynucléotides (ddNTPs), dépourvus de groupement 3'-OH.
Ainsi, l'incorporation d'un ddNTP stoppe l'élongation, générant des fragments d'ADN de tailles variables chacun terminé par un ddNMP spécifique.
Séquençage de Sanger automatisé
Il existe aujourd'hui une version automatisée du séquençage de Sanger.
- Les ddNTP sont marqués par des fluorophores distincts,
- la réaction est réalisée en un seul tube,
- les fragments sont séparés par électrophorèse capillaire,
- la séquence est visualisée sous forme d'un chromatogramme, dont la qualité permet d'évaluer la fiabilité de la lecture (rapport signal/bruit, chevauchement des pics).
Voir figure suivante.
Séquençage de deuxième génération (NGS)
En 2005 apparaissent de nouvelles technologies désignées sous l'acronyme NGS (pour Next-Generation Sequencing ou séquençage de nouvelle génération). Le NGS permet le séquençage massif et parallèle de millions d'ADN.
Elle repose sur :
- la fragmentation de l'ADN,
- une amplification clonale,
- une lecture simultanée de nombreux fragments.
Technologies majeures
La lecture des séquences se fait par :
- Séquençage par synthèse (Illumina)
Basé sur l'incorporation cyclique de nucléotides à terminaison réversible marqués par fluorescence. - Séquençage par ligature (SOLiD)
Basé sur des réactions de ligation successives.
Séquençage de troisième génération (TGS)
Le TGS permet le séquençage direct de molécules d'ADN sans amplification préalable.
Technologies majeures
Les principales technologies sont :
- PacBio SMRT (Single Molecule Real-Time): permet des lectures longues, adaptées aux inserts de grande taille.
- Oxford Nanopore: lecture par variation de courant électrique lors du passage de l'ADN à travers un nanopore.
Tableau comparatif
| Méthode | Avantages | Limites | Utilisation |
| Sanger | Lecture fiable | Faible débit, coût élevé | Validation de plasmide |
| NGS | Haut débit, coût réduit | Lectures courtes, analyse bioinformatique indispensable | Génomique globale |
| TGS | Très longues lectures | Taux d'erreur élevé, coût élevé | Grands inserts structures complexes |







